近日,研究所分布式供能与可在生能源实验室基于化学反应Gibbs自由能函数及![]() 方程,首次给出了Gibbs函数的热力学第二定律表述,建立了热流
方程,首次给出了Gibbs函数的热力学第二定律表述,建立了热流![]() 、化学反应Gibbs自由能与反应热
、化学反应Gibbs自由能与反应热![]() 的联系。该模型能够充分阐释热化学反应过程
的联系。该模型能够充分阐释热化学反应过程![]() 的演化规律,帮助理解热化反应
的演化规律,帮助理解热化反应![]() 与的相互作用。该方程从
与的相互作用。该方程从![]() 的角度为引发化学反应的各种情况建立了统一基准,首次揭示了各类化学反应的
的角度为引发化学反应的各种情况建立了统一基准,首次揭示了各类化学反应的![]() 本质。该研究成果为开展低温、高效的热化学反应提供了思路。
本质。该研究成果为开展低温、高效的热化学反应提供了思路。
引发化学反应的方法有很多,如电解反应、热解反应以及光催化等,然而目前国际上没有统一的分析方法能够阐明电解、热解以及光催化等途径的能量本质。其中,国际上通用的化学反应进行方向的判据为Gibbs自由能判据。然而Gibbs自由能判据不能阐明化学反应进行的能量本质,也不能给出非自发反应到自发反应的![]() 差距。
差距。
工程热物理研究所率先开展了这方面的研究工作,以目前发展潜力较大的热化学循环分解水制氢体系为研究对象,建立了化学反应![]() 与品位方程,阐明了反应过程中能质转化与品位变化的本征规律,给出了通过调整反应熵以及外界补偿
与品位方程,阐明了反应过程中能质转化与品位变化的本征规律,给出了通过调整反应熵以及外界补偿![]() 改善化学反应热力学性能(如降低反应温度)的方法。研究发现化学反应本质上是
改善化学反应热力学性能(如降低反应温度)的方法。研究发现化学反应本质上是![]() 到的退化过程。当反应焓所携带的
到的退化过程。当反应焓所携带的![]() 大于反应需要的
大于反应需要的![]() 时,化学反应自发进行;反之,为非自发反应。改变反应熵可以降低化学反应的
时,化学反应自发进行;反之,为非自发反应。改变反应熵可以降低化学反应的![]() 要求,从而在较低的温度下触发化学反应;外界提供的能量同样可以触发反应,但是所提供的能量与其品位以及反应温度有关。
要求,从而在较低的温度下触发化学反应;外界提供的能量同样可以触发反应,但是所提供的能量与其品位以及反应温度有关。
研究工作得到了国家自然科学基金优秀青年项目(NO.51722606)、基础科学中心项目(NO.51888103)的支持,相关研究成果发表在Energy(2021, 219: 119531)上。
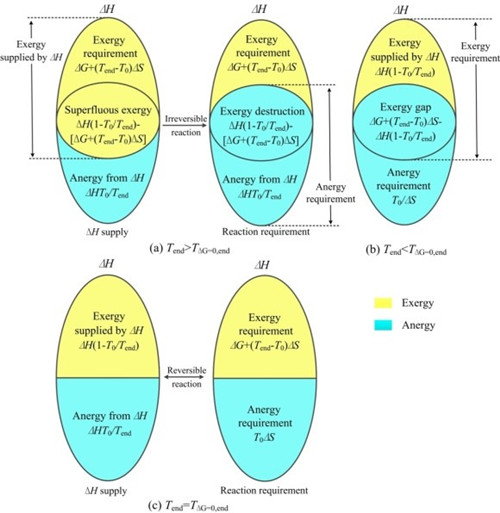
图1 吸热反应过程![]() 的演化规律
的演化规律
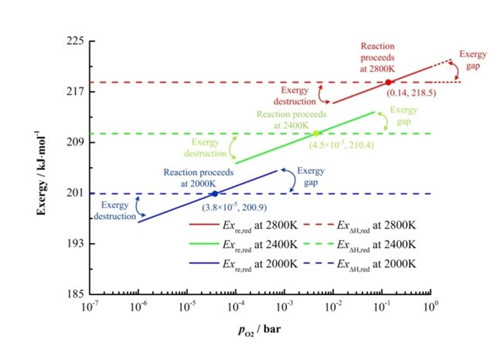
图2 反应需求![]() 与压力的关系
与压力的关系
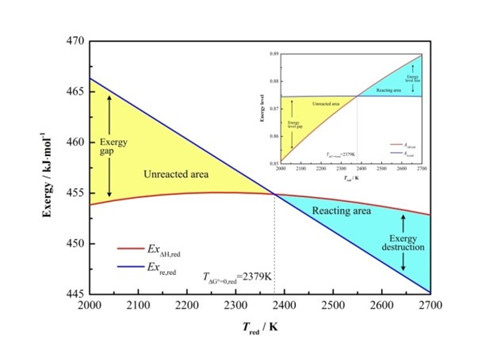
图3 输入![]() 、反应需求
、反应需求![]() 与温度的关系
与温度的关系